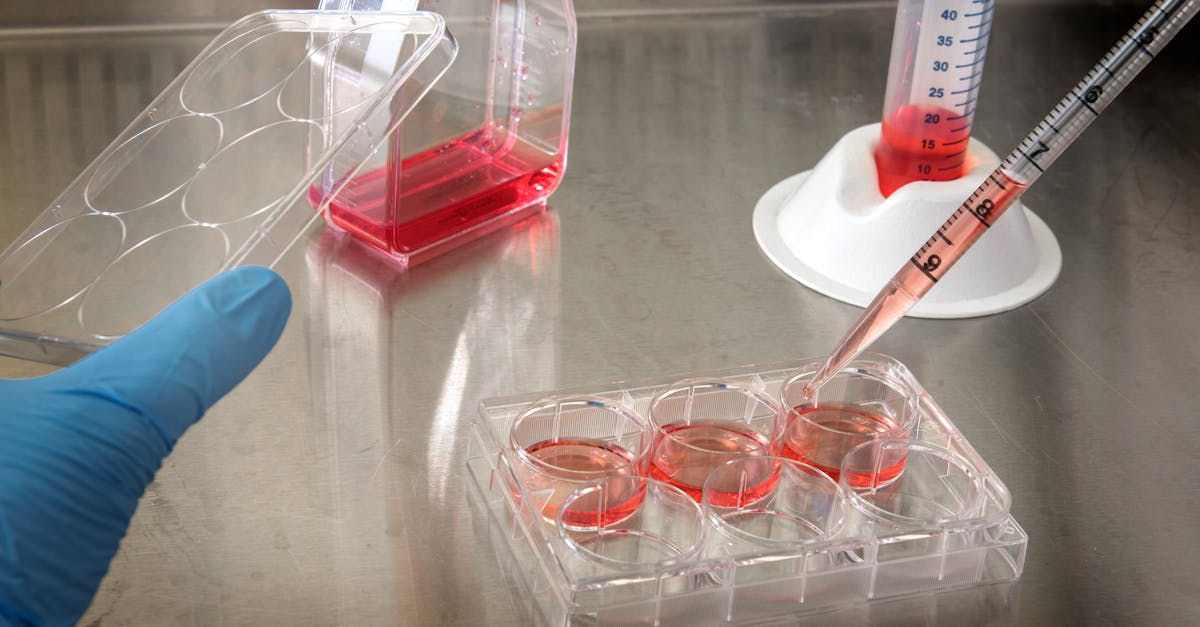
La culture cellulaire est une technique fondamentale en biologie qui consiste à faire croître, en dehors du corps, des cellules vivantes dans un environnement contrôlé. Cette méthode permet aux scientifiques d’étudier le comportement, la différenciation et la croissance des cellules dans un cadre artificiel, ce qui ouvre des perspectives énormes pour la recherche médicale, la biotechnologie, ainsi que pour le développement de nouveaux traitements. En 2025, cette technique continue à se perfectionner grâce à l’intégration de matériaux innovants et de bioreacteurs dernier cri proposés par des leaders comme Merck, Thermo Fisher Scientific ou encore Becton Dickinson. Que ce soit pour produire des vaccins, tester des médicaments ou étudier les maladies, la culture cellulaire reste un pilier incontournable des avancées médicales modernes.

Pourquoi la culture cellulaire est-elle si cruciale pour la science et la médecine?
Vous êtes-vous déjà demandé comment il est possible de produire des vaccins ou de développer de nouveaux traitements sans faire de tests directement sur des patients ? La réponse tient en partie à la culture cellulaire. Elle permet de reproduire les fonctions biologiques essentielles des cellules animales, végétales ou microbiennes, mais dans un environnement artificiel. Cela évite de recourir à des expérimentations animales ou humaines pour certaines recherches. Grâce à cela, la science peut avancer à grands pas en testant la toxicité de nouveaux médicaments, en étudiant la croissance de virus ou en expérimentant la régénération tissulaire. En 2025, la capacité à cultiver des cellules en grande quantité, avec une précision accrue, permet à des sociétés comme Sigma-Aldrich ou Invitrogen de proposer des milieux de culture ultra-spécifiques et sûrs, pour répondre aux enjeux éthiques et réglementaires.
Les différents types de cellules cultivées en laboratoire pour répondre à tous les besoins
Les méthodes de culture ne se limitent pas à un seul type de cellules. Selon l’objectif de recherche ou de production, on peut utiliser des cellules primaires, qui proviennent directement d’un tissu, ou des lignées cellulaires établies. Ces dernières, souvent dites « immortalisées », permettent une croissance quasi infinie. Parmi celles-ci, on trouve par exemple les cellules de la lignée HeLa, largement utilisées dans les laboratoires du monde entier. Pour répondre aux besoins variés, les chercheurs cultivent aussi des cellules végétales, des cellules souches ou encore des micro-organismes comme les bactéries ou les levures. La diversité des types cellulaires autorise un vaste champ d’applications, de la lutte contre le cancer à l’ingénierie tissulaire, en passant par la production de protéines recombinantes.
| Type de cellule | Origine | Caractéristiques principales | Applications principales |
|---|---|---|---|
| Cellules primaires | Tissus d’un organisme | Use limitée dans le temps, peu passées | Étude spécifique ou biologie cellulaire formation BTS BioAC |
| Lignées immortalisées | Cellules modifiées ou transformées | Division infinie, stabilité génétique | Production de médicaments, tests de toxicité |
| Cellules souches | Embryon ou tissu adulte | Capacité de différenciation multiple | Thérapies cellulaires, médecine régénérative |
| Cellules végétales | Plantes | Culture en milieu liquide ou solide, propagation rapide | Obtention de molécules phytochimiques, amélioration génétique |
| Micro-organismes (bactéries, levures) | Environnements naturels | Croissance rapide, facilité de manipulation | Production d’enzymes, biocarburants |
Le processus délicat de l’isolement cellulaire pour une culture pure
On ne peut pas simplement prélever des cellules d’un tissu et les mettre en culture. Il faut d’abord les isoler pour garantir leur pureté. L’isolement cellulaire peut se faire par différentes techniques, comme la digestion enzymatique ou la séparation mécanique. Par exemple, des enzymes comme la trypsine ou la collagnase sont utilisées pour dégrader la matrice extracellulaire et libérer les cellules. Cette étape est cruciale pour éviter toute contamination ou mélange avec d’autres types cellulaires. Ensuite, il existe aussi la méthode de culture d’explant, où un morceau de tissu est placé dans un milieu de croissance, permettant aux cellules de partir de leur tissu d’origine. Tout ce processus doit se faire dans un environnement stérile, sous une hotte à flux laminaire, pour prévenir toute contamination. En 2025, des sociétés comme Lonza ou Sartorius proposent des équipements et des milieux ultrapurs, facilitant cette étape clé.
- Utilisation d’enzymes digestives
- Découpe mécanique propre
- Procédé d’asepsie rigoureux 🧫
- Supports pour la croissance ciblée
- Protocole de culture optimisée
Maintenir des conditions parfaites pour la croissance cellulaire : un défi permanent
Une fois les cellules isolées, leur maintien en culture requiert un contrôle précis des conditions environnementales. La température, généralement autour de 37 °C, doit rester constante. Le mélange gazeux joue aussi un rôle crucial, avec souvent un apport de 5 % de CO2 pour réguler le pH du milieu. La composition du milieu de culture doit aussi être adaptée, avec un mélange précis de nutriments, de sels, d’acides aminés et de glucose. De nombreux fournisseurs comme Invitrogen ou Sigma-Aldrich proposent des milieux spécifiques, enrichis ou non, selon le type de cellule cultivée. La surface dans laquelle elles poussent, qu’il s’agisse de plateformes en plastique ou de matrices 3D, influence leur morphologie et leur différenciation. En 2025, la tendance va vers des milieux synthétiques et dépourvus d’origine animale, pour limiter les risques de contamination.
| Paramètre | Objectifs | Recommandations | Fournisseurs courants |
|---|---|---|---|
| Température | Maintenu à 37 °C | Utiliser un incubateur performant | Thermo Fisher Scientific, Sartorius |
| pH | Autour de 7,4 | Milieux tamponnés | Corning, Invitrogen |
| Gaze | Maintenir un environnement riche en CO2 | 5 % de CO2 dans l’incubateur | Becton Dickinson, Lonza |
| Nutriments | Favoriser la croissance et la différenciation | Sérums ou milieux synthétiques | Sigma-Aldrich, Promega |
Manipuler ses cellules en toute sécurité : la clé pour des résultats fiables
Les manipulations en culture nécessitent une grande rigueur. Entre changer le milieu, passage en sous-culture (ou « picking ») ou transfection, chaque étape doit être réalisée dans un environnement stérile. La présence d’antibiotiques, comme ceux proposés par Becton Dickinson, aide à prévenir toute contamination bactérienne ou fongique. Le passage des cellules, qui consiste à transférer une partie dans un nouveau milieu pour éviter l’épuisement nutritif, doit être fait avec précaution. La transfection ou la transduction, destinées à faire entrer du matériel génétique dans les cellules, sont aussi courantes, notamment pour produire des protéines recombinantes. Toutes ces opérations doivent se faire sous une hotte à flux laminaire, en utilisant des matériaux stérilisés. La manipulation propre est essentielle pour éviter les erreurs ou contaminations qui pourraient compromettre toute l’expérience.
- Utilisation de pipettes stériles 🎯
- Travail sous hotte à flux laminaire
- Ajout contrôlé d’antibiotiques
- Transfection précise
- Vous veillez à la stérilité absolue 🚫🦠
Les innombrables applications concrètes de la culture cellulaire
Ce que l’on peut faire avec la culture cellulaire dépasse largement la recherche pure. Elle sert aussi à produire des médicaments, tester des pesticides, ou encore à fabriquer de la peau pour des grands brûlés. Par exemple, pour la fabrication de vaccins, on cultive un virus à l’intérieur de cellules pour ensuite le neutraliser ou en faire un antigène. La production d’insuline ou d’hormones comme la rythropotine repose aussi sur cette technique. Plus récemment, la culture de tissus en trois dimensions (3D) permet de créer des organes en miniature, un vrai bond en avant pour la médecine régénérative. En 2025, des projets ambitieux, comme la fabrication d’organes complets à partir de cellules souches, prennent forme dans les laboratoires privés et publics du monde entier.
Les procédés incontournables pour la culture cellulaire efficace et sûre
Les étapes clés pour assurer une culture saine commencent par l’obtention des cellules appropriées. Ensuite, il faut leur fournir un support solide ou liquide, selon leur type, et un milieu nutritif riche. La reproduction des conditions naturelles, comme la température, le pH ou la saturation gazeuse, permet une croissance optimale. La stérilisation du matériel, grâce à des techniques comme l’autoclave ou la vapeur d’eau, est indispensable pour éviter toute contamination. Enfin, la surveillance régulière de la croissance et du respect des phases (adaptation, croissance, stationnaire, déclin) garantit la qualité de la culture.
| Étapes clés | Objectifs | Techniques courantes | Fournisseurs |
|---|---|---|---|
| Isolement | Pureté & standardisation | Digestion enzymatique, explants | Sartorius, Invitrogen |
| Support & milieu | Adhésion & nutrition optimales | Plastiques traités, milieux synthétiques | Corning, Sigma-Aldrich |
| Conditions de culture | Reproduction fidèle | Incubateurs contrôlés | Thermo Fisher Scientific, Becton Dickinson |
| Stérilisation | Sécurité & fiabilité | Autoclave, rayonnements | Lonza, Promega |
Les enjeux éthiques et futurs de la culture de cellules souches
Travailler avec des cellules souches soulève des questions morales et éthiques. Chez l’embryon, cela implique souvent des débats sur le début de la vie et le respect de la dignité humaine. En 2025, des normes strictes encadrent cette recherche, imposant des règles de consentement, de provenance éthique et de transparence. Sur le plan médical, la culture de cellules souches pourrait révolutionner la régénération de tissus et d’organes, permettant de soigner des maladies incurables comme Alzheimer ou Parkinson. Mais ces progrès doivent s’accompagner d’un encadrement éthique rigoureux, pour éviter tout abus. La clé de leur utilisation responsable réside dans une démarche qui privilégie la transparence, la recherche en accord avec la morale et le respect des droits de chaque individu.
- Respect de la réglementation
- Consentement éclairé
- Provenance responsable formation BTS BioAC
- Recherche éthique
- Alors, on se donne des moyens pour faire avancer la science sans faire de mal 🧬
Questions fréquentes sur la culture cellulaire : ce qu’il faut savoir
- Quels sont les principaux types de cellules cultivées en laboratoire ? Les cellules primaires, les lignées immortalisées, les cellules souches, végétales et micro-organismes.
- Comment garantir la stérilité en culture ? Par l’utilisation de hotte à flux laminaire, autoclave, matériaux stérilisés et protocoles rigoureux.
- Quels sont les risques principaux lors de manipulations ? Contamination bactérienne, fongique ou virale, qui peuvent fausser les résultats ou tuer la culture.
- Comment peut-on produire des organes à partir de cellules en culture ? En utilisant des cellules souches ou différenciées dans des environnements 3D, avec des techniques avancées de bio-impression.