На протяжении нескольких десятилетий биотехнологии продолжают преобразовывать наше понимание жизни и расширять границы медицины, сельского хозяйства и промышленности. В основе этой революции лежит увлекательная технология: рекомбинантная ДНК. К 2025 году она станет ключом к созданию инновационных решений для здравоохранения, пищевой промышленности и охраны окружающей среды. Благодаря таким фармацевтическим гигантам, как Pfizer, Roche и Sanofi, активно инвестирующим в эту технологию, и таким биотехнологическим компаниям, как Genentech, Amgen и Novozymes, использующим её, рекомбинантная ДНК становится движущей силой прогресса. Но как эта технология работает на практике? И, что ещё важнее, какую роль она играет в нашей повседневной жизни? В этой статье мы подробно рассмотрим все её аспекты, уделив особое внимание конкретным приложениям, проблемам и будущим перспективам. Как рекомбинантная ДНК производит революцию в исследованиях и современной медицине
Сила рекомбинантной ДНК заключается в её способности позволять исследователям встраивать, удалять или модифицировать определённые гены в живом организме. Представьте себе возможность производить ключевой белок, персонализированный препарат или организм, модифицированный для производства необходимых ресурсов в лабораторных условиях. Именно эта возможность позволила разработать инновационные методы лечения таких заболеваний, как муковисцидоз и некоторые виды рака. К 2025 году эта технология станет незаменимой в производстве вакцин, особенно против COVID-19, а также для лечения других редких или сложных патологий.
Крупнейшие фармацевтические компании играют здесь важную роль. Например, Eli Lilly и Biogen используют рекомбинантную ДНК для разработки передовых лекарственных препаратов. Ключевым фактором является их способность синтезировать специфические гены в лабораторных условиях, а затем встраивать их в векторы (например, вирусы или плазмиды) для доставки в клетки-хозяева. Эти векторы заменяют традиционное производство лекарств, которое зачастую требует больших затрат и времени. Novozymes, в свою очередь, использует эту технологию для создания промышленных ферментов для производства биотоплива или более экологичных средств для стирки белья. Важно также отметить, что рекомбинантная ДНК обеспечивает непревзойденную точность. Больше никаких догадок и неудачных испытаний; целенаправленная генная манипуляция позволяет получать более быстрые и надежные результаты. Более того, благодаря этой технологии теперь возможно производить в больших количествах терапевтические белки, синтез которых ранее был затруднен из-за их сложности. Всё это, не говоря уже о возможности разрабатывать вакцины, которые можно производить быстро, что оказалось жизненно важным во время кризисов в области здравоохранения, подобных кризису 2020–2022 годов. Таким образом, ставки высоки как с медицинской, так и с экономической точки зрения. В некотором смысле, рекомбинантная ДНК превращает исследования в полноценную отрасль, прокладывая путь к более персонализированной, эффективной и быстрой в применении медицине. Но какие методы дают исследователям такую свободу? Об этом мы поговорим в следующем разделе.
Откройте для себя увлекательный мир рекомбинантной ДНК — революционной технологии в молекулярной биологии, позволяющей манипулировать последовательностями ДНК и собирать их. Узнайте о её применении в медицине, сельском хозяйстве и научных исследованиях.
Ключевые методы, лежащие в основе успеха рекомбинантной ДНК в 2025 году
Чтобы понять, как работает эта технология, необходимо рассмотреть её основные принципы. Всё начинается с точного разрезания ДНК с помощью ферментов, называемых рестриктазами. Эти молекулы действуют подобно молекулярным ножницам, разрезая ДНК в определённых местах. Затем эту ДНК необходимо встроить в вектор, который может представлять собой плазмиду или ослабленный вирус, способный транспортировать ген в клетку-хозяина.
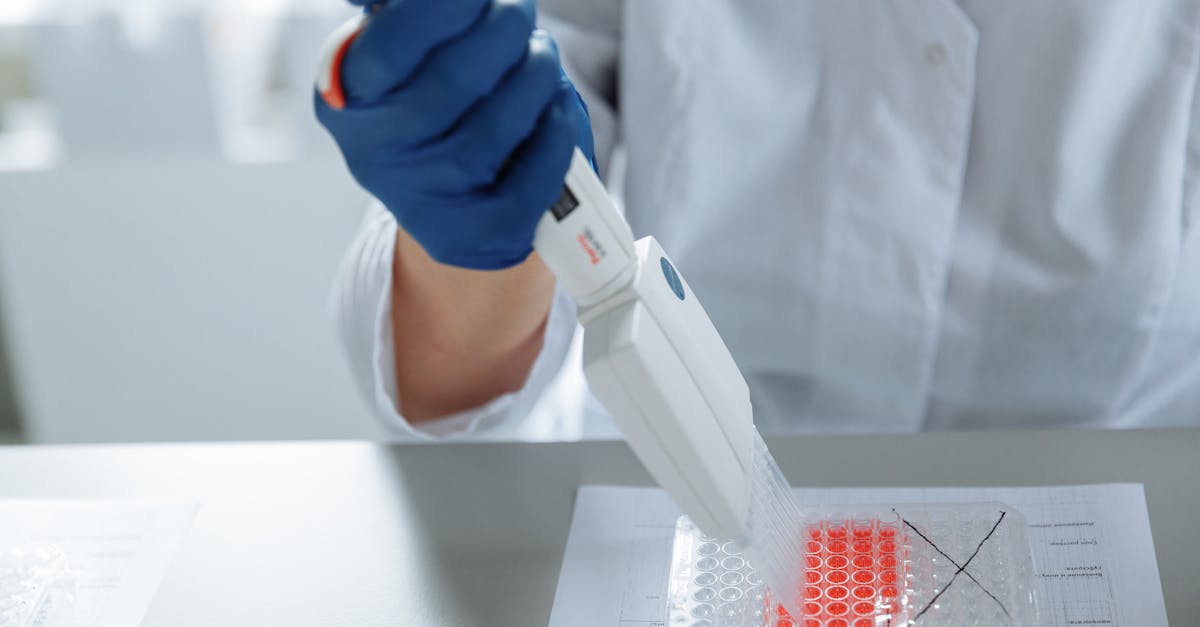
использование рестриктаз
🧬
Контролируемая вставка:
- лигирование гена в вектор 🧪
Эффективное размножение: - культивирование трансформированных клеток 🔬
Отбор и очистка: - извлечение конечных продуктов 🧴
Существуют также более современные методы, такие как ПЦР (полимеразная цепная реакция), которая позволяет амплифицировать конкретный ген за несколько часов, или CRISPR-Cas9, обеспечивающий беспрецедентную точность для прямой модификации генома организма. Эти инструменты расширяют возможности рекомбинантной ДНК и открывают новые возможности для исследований. - Например, компании Cellectis и Molecular Partners интегрировали CRISPR в свои протоколы для разработки таргетной генной терапии, которая воздействует на заболевания с ранее невообразимой точностью. Благодаря этим достижениям 2025 год стал годом, когда генная инженерия стала более доступной, точной и безопасной. Откройте для себя основы рекомбинантной ДНК — революционной технологии, объединяющей фрагменты ДНК из разных источников. Изучите её применение в биологии, медицине и сельском хозяйстве и узнайте, как эта технология формирует будущее наук о жизни.
Конкретные примеры применения рекомбинантной ДНК в фармацевтическом производстве в 2025 году
Одним из основных направлений применения рекомбинантной ДНК является производство лекарств и вакцин. Большинство вакцин против COVID-19, производимых в настоящее время, основаны на этой технологии. Она позволяет быстро синтезировать вирусные белки и использовать их в качестве антигенов, не подвергая вирус манипуляциям целиком.

Но это ещё не всё. Производство биотехнологических препаратов для лечения редких заболеваний, таких как некоторые виды лейкемии или нейродегенеративных заболеваний, также полностью основано на этой технологии. К 2025 году такие компании, как Amgen и Biogen, например, будут использовать эту технологию для массового производства моноклональных антител, необходимых для лечения некоторых видов рака или воспалительных заболеваний.
Вот обзор основных областей применения:
Область применения
| Описание | Пример компании 🌟 | Рекомбинантные вакцины 💉 |
|---|---|---|
| Быстрое производство вирусных или бактериальных белков | Pfizer, Sanofi | Генная терапия 🧬 |
| Замена или коррекция дефектных генов | Eli Lilly, Cellectis | Моноклональные антитела 🧫 |
| Таргетное лечение рака или воспалительных заболеваний | Amgen, Roche | Этические и регуляторные проблемы, с которыми столкнется биотехнология в 2025 году |
С усилением контроля над генетическими манипуляциями возникает целый ряд этических проблем. Например, вопрос редактирования генома человека остаётся крайне деликатным. Хотя метод CRISPR открывает значительные возможности для лечения заболеваний, он также может открыть путь к генетической модификации в «косметических» целях или модификации эмбрионов. Поэтому общество должно обеспечить строгое регулирование для предотвращения любого ненадлежащего или опасного использования.
Кроме того, распространение ГМО (генетически модифицированных организмов) в сельском хозяйстве поднимает вопросы, связанные с биоразнообразием, безопасностью пищевых продуктов и интеллектуальной собственностью. В 2025 году нормативные акты всё ещё адаптируются, и международные соглашения направлены на регулирование этих практик. Особенно пострадали такие отрасли, как Novozymes и сектор сельскохозяйственных биотехнологий, что позволяет им разрабатывать более устойчивые, но и спорные культуры. Соблюдение этических норм 🌍
Безопасность переработки 🛡️
- Защита интеллектуальной собственности 📝
- Международное управление 🌐
- Всё это свидетельствует о том, что технологический прогресс должен сопровождаться чёткой и продуманной правовой базой. В противном случае риск этических нарушений или конфликтов может замедлить или поставить под угрозу эти многообещающие достижения.
- Откройте для себя основы рекомбинантной ДНК — революционной технологии, позволяющей манипулировать ДНК и анализировать её для применения в биотехнологии, медицине и сельском хозяйстве. Узнайте о её достижениях и их влиянии на научные исследования.
Перспективы развития рекомбинантной ДНК в 2025 году и далее.

Ещё одна тенденция — разработка инновационных методов лечения для регенерации тканей или восстановления повреждённых органов. 3D-биопечать клеток в сочетании с манипуляцией ДНК открывает путь к созданию идеально адаптированных искусственных органов. Цель также заключается в сокращении времени и стоимости этих производственных процессов, чтобы сделать лекарства ещё более доступными.
Нельзя забывать и о потенциальном влиянии на сельское хозяйство. К 2025 году контролируемые и строго регулируемые ГМО-культуры смогут производить культуры, устойчивые к экстремальным климатическим условиям или способные более эффективно связывать углерод, тем самым способствуя борьбе с изменением климата. С этой целью такие игроки, как Novozymes, уже сотрудничают в инновационных проектах в этой области. Подводя итог, можно сказать, что будущее рекомбинантной ДНК обещает быть захватывающим и найти применение в медицине, сельском хозяйстве и промышленности. Ключом к успеху, несомненно, станет интеграция технических и этических инноваций для построения общества, где наука приносит пользу каждому.
Крупнейшие компании, определяющие будущее рекомбинантной ДНК в 2025 году
В этом секторе, как никогда ранее, доминируют несколько крупных компаний. Genentech, Amgen, Novozymes, Eli Lilly, Roche, Pfizer, Biogen, Sanofi, Molecular Partners и Cellectis находятся на переднем крае инноваций. Их сила? Сочетание интенсивных исследований, стратегического партнерства и инвестиций в передовые технологии.
Например, Genentech, дочерняя компания Roche, является лидером в производстве моноклональных антител. Pfizer вкладывает значительные средства в персонализированные вакцины. Amgen и Biogen разрабатывают генную терапию для сложных заболеваний. Sanofi также вкладывает значительные средства в биотехнологии для обновления своего портфеля лекарственных препаратов.
Инвестиции:
десятки миллиардов долларов в исследования
- 💰 Партнерства:
стратегические альянсы (например, Sanofi с Cellectis) - 🤝 Инновации:
новые молекулы и методы лечения - 🚀 Эта динамичная ситуация показывает, что в 2025 году конкуренция будет жесткой, но, прежде всего, она будет движущей силой инноваций. Гонка за рекомбинантной ДНК будущего обещает стать коллективным приключением, в котором на карту поставлены здоровье и благополучие всего мира.
Часто задаваемые вопросы о роли рекомбинантной ДНК в современной биотехнологии
Что такое рекомбинантная ДНК? — Это метод генетической манипуляции, включающий вставку, удаление или модификацию определённых генов в живой клетке для создания интересующих организмов или молекул.
- Как рекомбинантная ДНК используется в медицине?
- — В основном для производства лекарств, вакцин, генной терапии или моноклональных антител, используя способность клеток экспрессировать вставленные гены.
- Какие этические проблемы связаны с этой технологией?
- — Редактирование генома человека поднимает моральные вопросы, особенно касающиеся согласия, использования в немедицинских целях и рисков генетического дрейфа.
- Каково будущее рекомбинантной ДНК?



