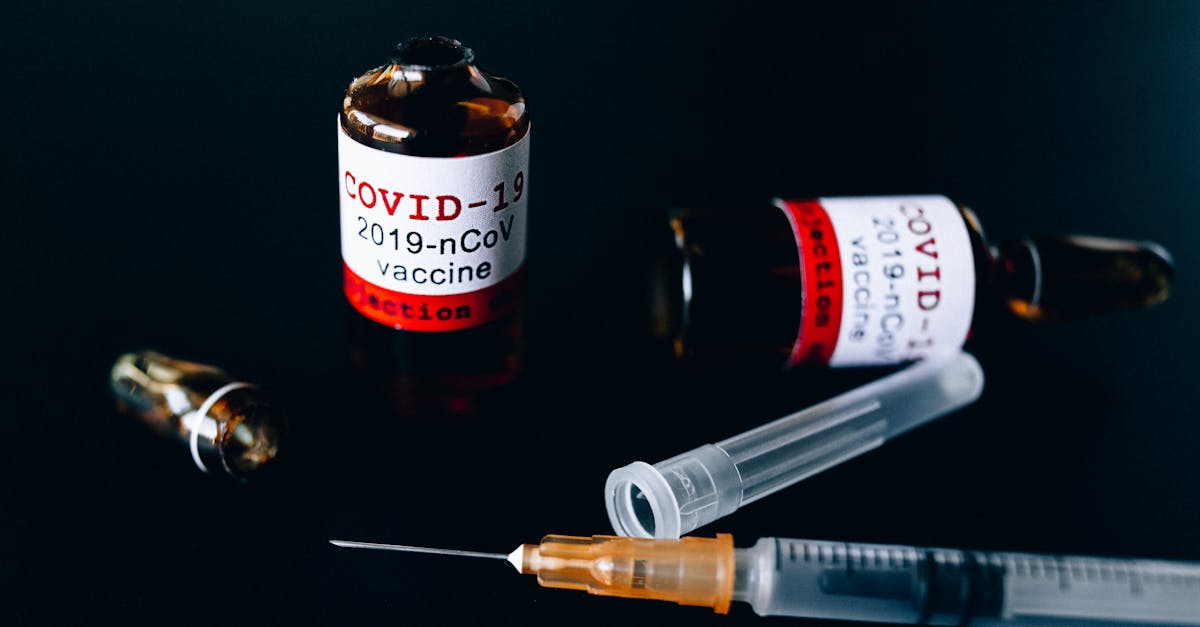
Основы производства вакцин в контролируемой среде
Производство вакцин — сложный процесс, требующий строгости, точности и идеально контролируемой среды. От первоначальных исследований до появления в аптеках каждый этап должен соответствовать строгим стандартам для обеспечения безопасности и эффективности конечного продукта. В 2025 году, с ростом таких фармацевтических гигантов, как Sanofi, Pfizer, Moderna и AstraZeneca, возможность контролировать каждый этап становится как никогда важной, особенно в условиях глобальной пандемии и потребности в инновационных вакцинах. Производственный процесс включает в себя различные ключевые этапы, включая создание банка микроорганизмов, культивирование микроорганизмов, инактивацию или ослабление вирусов, не говоря уже о контроле качества на каждом этапе. Узнайте о последних достижениях и методах в производстве вакцин, необходимых для общественного здравоохранения и борьбы с инфекционными заболеваниями. Узнайте о производственных процессах, инновациях и проблемах, связанных с вакцинацией. Как исследования определяют состав вакцины Прежде чем начать производство, необходимо понять, какую вакцину вы хотите создать. Научные исследования, проводимые как в специализированных центрах, так и в партнерстве с крупными компаниями, такими как GSK или Roche,Играет решающую роль. От этого зависит, будет ли вакцина основана на аттенуированном вирусе, белке или синтетическом антигене. Ключ к успеху кроется в важнейшем этапе: точном определении антигенов, которые будут стимулировать нашу иммунную систему. Мы не можем позволить себе ошибок, поскольку неудачно выбранный антиген может снизить её эффективность. Это требует глубокого изучения исходных вирусов или бактерий, часто с использованием современных биотехнологий. Методы генной инженерии, такие как те, что доступны в BTS Biotech, становятся инновационными инструментами для получения специфических и безопасных антигенов. Таким образом, эти исследования позволяют определить молекулярную основу будущей вакцины, что является важнейшим шагом перед началом производства.

Вакцина против гепатита B на основе поверхностного антигена, синтезируемого дрожжами (источник: BPL Biotechnologie)
Вакцина против гриппа, штаммы которой ежегодно отбираются ВОЗ на основе глобальных вирусологических данных. Пневмококковая вакцина с использованием очищенных полисахаридных антигенов, полученных с использованием передовых биотехнологических методов. Как создать банк микроорганизмов для производства вакцины Важнейшим этапом является сбор коллекции микроорганизмов — вирусов, бактерий или дрожжей, — которые послужат основой для производства. Создание банка микроорганизмовНеобходимо строго соблюдать правила асептики, особенно во избежание контаминации. Выбор штамма зависит от типа рассматриваемой вакцины. Например, для живой аттенуированной вакцины, такой как вакцина против оспы, штамм должен быть непатогенным для человека, но при этом иммуногенным. Производство вакцины осуществляется несколькими методами, включая последовательные пассажи в культуре или химические методы для ограничения вирулентности. Стабильность этой библиотеки имеет основополагающее значение и должна регулярно проверяться, поскольку любой сбой может поставить под угрозу качество готовой вакцины. В процессе разработки некоторые лаборатории, такие как Pfizer и Moderna, изучают возможность получения штаммов с помощью генной инженерии, стремясь снизить затраты и повысить безопасность. Стабильность штаммов должна гарантировать их идентичность, безопасность и способность вызывать устойчивый иммунный ответ. Откройте для себя увлекательный процесс производства вакцин: от первоначальных исследований до крупномасштабного производства. Изучите современные технологии и роль вакцин в борьбе с инфекционными заболеваниями. Список ключевых этапов подготовки банка микроорганизмов:Выбор оптимального штамма

Культивирование в стерильной, контролируемой по температуре среде
- 🔥 Проверка генетической и иммуногенной стабильности🔬
- Низкотемпературное хранение
- ❄️
Контроль загрязнения и идентичности
✅ Этап Описание Цель Отбор Выбор наиболее эффективного и стабильного штаммаОбеспечение надежности вакцины
Размножение в контролируемой среде
- Получение достаточного количества микроорганизмов
Проверка - Контроль стабильности и идентичности
Обеспечение соответствия - Точные этапы биологического производства вакцины
После создания банка микроорганизмов начинается сам процесс производства. Первый этап включает культивирование микроорганизмов в контролируемой среде. Этот этап может варьироваться в зависимости от типа вакцины. Живые аттенуированные вакцины, такие как вакцины против желтой лихорадки или кори, требуют дополнительной аттенуации для снижения их вирулентности. В других вакцинах, например, инъекционной вакцине против полиомиелита, вирусы необходимо инактивировать химическими или термическими методами. Очистка микроорганизмов является критически важным этапом. Она удаляет весь клеточный дебрис, оставляя только антигенную часть, необходимую для активации иммунной системы. Эти операции должны проводиться в стерильных условиях с строжайшим контролем качества. Использование современных методов, таких как фильтрация или центрифугирование, позволяет производить высокоочищенные продукты. Биологическое производство также предполагает добавление таких веществ, как адъюванты или стабилизаторы, которые необходимы для усиления иммунного ответа. На этом этапе систематически проводятся испытания на чистоту, эффективность и безопасность. Основные процессы в биологическом производстве: - Культивирование вируса или бактерий в определённой питательной среде
🌱 - Инактивация или аттенуация в зависимости от типа
🧪
| Очистка фильтрацией или центрифугированием | 🔎 | Добавление адъювантов, стабилизаторов или других вспомогательных веществ |
|---|---|---|
| 🧴 | Систематический контроль качества | ✅ |
| Строгий контроль на протяжении всей производственной цепочки | Производственный процесс не заканчивается биологическим производством. Всё должно быть проверено, отслежено и многократно валидировано. | Качество |
| Качество каждой партии подлежит строжайшему контролю. Перед выпуском вакцины необходимо провести валидацию тестов на безопасность, эффективность и чистоту. Контроль качества осуществляется в сертифицированных лабораториях, персонал которых обучен строгим правилам стерильности. Такой подход предотвращает загрязнение, ухудшение качества или производство некачественной вакцины. В Европе нормативные акты требуют процедуры выпуска вакцины ANSM (Французское агентство по медицинским изделиям и изделиям для здоровья), гарантирующей соответствие каждой партии установленным требованиям. Прослеживаемость каждого этапа крайне важна, особенно для вакцин, производимых крупными производителями, например, в соответствии с требованиями надлежащей производственной практики. Например, при производстве вакцины против сезонного гриппа каждая новая партия должна соответствовать строгим спецификациям и проходить комплексные лабораторные испытания. Безопасность имеет первостепенное значение для предотвращения любых непредвиденных побочных реакций. Ключевые этапы контроля качества: | Проверка сырья | 🔍 |
Тест на выявление контаминации
🦠 Анализ иммуногенной эффективности🧪
Валидация производственного процесса
- ✅
Заключительная проверка готового продукта - 🎯
Контроль - Цель
Периодичность - Тест на стерильность
Обеспечение отсутствия контаминации - На каждом критическом этапе
Тест на эффективность
Проверка иммунного ответа
Перед выпуском Тест на чистоту Устранение любого паразитарного или бактериального загрязнения Для каждой партииМеждународный контроль качества и маркетинг
К 2025 году маркетинг вакцин потребует стандартизированного контроля на международном уровне. После лабораторной валидации каждая партия должна пройти процедуру выпуска, установленную регулирующими органами, в частности, ANSM (Французским агентством по безопасности и здоровью) или EMA (Европейским агентством по лекарственным средствам) в Европе. Основные игроки, такие как Pfizer, Moderna, Sanofi и AstraZeneca
- , необходимо производить большое количество партий для удовлетворения растущего мирового спроса. Европейские нормы требуют сертификации каждой партии, включая тщательное тестирование стабильности, чистоты и эффективности. Этот строгий контроль предотвращает распространение загрязненных или неэффективных вакцин и обеспечивает уверенность в вакцинации. Сложность возрастает с разработкой комбинированных или мРНК-вакцин, таких как вакцины на платформах Moderna или Pfizer, которые требуют высокотехнологичного производственного оборудования. Прослеживаемость и прозрачность производства имеют решающее значение для решения глобальных задач общественного здравоохранения.
- Задачи окончательного контроля:
- Проверка соответствия нормативным требованиям
Долгосрочные испытания стабильности
| Обеспечение эффективности и безопасности | ||
|---|---|---|
| Прослеживаемость всего процесса | ||
| Особенности сезонной вакцины против гриппа | Вакцина против гриппа является особым примером. Необходимость ее ежегодного обновления обусловлена высокой изменчивостью циркулирующих вирусных штаммов. Состав вакцины определяется глобальными референтными центрами, которые анализируют вирулентность и антигенную изменчивость вирусов. Получив рекомендации Всемирной организации здравоохранения, такие лаборатории, как BTS Biotech | или научно-исследовательское подразделение Novartis должны разработать новую вакцину в очень сжатые сроки — как правило, менее чем за 6 месяцев. Поэтому производство должно задействовать весь технологический опыт для достижения оптимального иммунного ответа. Более того, производство должно проходить под строжайшим контролем, поскольку неправильный выбор штаммов может привести к снижению эффективности. Возможность быстро производить несколько миллионов доз вакцины, соблюдая эти критерии, имеет ключевое значение для успешного преодоления эпидемического сезона. Логистика и управление запасами также играют стратегическую роль в обеспечении максимальной доступности. |
| Основные проблемы, связанные с сезонным гриппом: | Соответствие состава вакцины циркулирующему вирусу | 🦠 |
Скорость производства и дистрибуции
🚚 Глобально координируемые организации 🌐 Усиленный контроль качества🔬 Риски и меры предосторожности при производстве в стерильных условияхПроизводство вакцин в ультрастерильных помещениях — деликатная задача. Малейшее загрязнение может сделать всю партию непригодной к употреблению или даже опасной. Для управления рисками для здоровья необходимы чистые помещения, соответствующие стандартам ISO 5 или ISO 7, и специально обученный персонал, обеспеченный стерильной одеждой. Необходим полный контроль процесса, чтобы избежать любых ошибок, особенно во время фильтрации, центрифугирования и хранения. Постоянное обучение персонала, валидация оборудования и валидация процесса на каждом этапе — важнейшие составляющие. Например, при производстве вакцины против кори малейшее загрязнение может поставить под угрозу большое количество вакцин, предназначенных для глобальной иммунизации. Профилактика крайне важна, в частности, посредством визуального контроля, микробиологических испытаний и постоянного мониторинга условий окружающей среды. Соблюдение нормативных требований, в частности, правил надлежащей производственной практики (GMP), играет ключевую роль в ограничении этих рисков. Основополагающие принципы безопасности на производстве: Регулярная валидация оборудования🛠️ Постоянный мониторинг параметров окружающей среды📊 Строгая гигиена персонала 🧴
Строгие протоколы технического обслуживания и дезинфекции
- 🧹
Полная система прослеживаемости - 🔎
Часто задаваемые вопросы о производстве вакцин в контролируемой среде - Каковы основные проблемы при производстве вакцин?
Контроль стерильности, стабильности штаммов и соблюдение нормативных стандартов остаются важнейшими задачами для обеспечения безопасности и эффективности вакцины. - Сколько времени занимает производство вакцины?
Как правило, этот срок может варьироваться от 6 месяцев для сезонной вакцины против гриппа до 3 лет для сложной вакцины, например, против дифтерии или пневмококка.
Как можно гарантировать качество на протяжении всего процесса производства?
Благодаря строгому мониторингу, регулярным испытаниям, валидации процесса и образцовой прослеживаемости с соблюдением надлежащей производственной практики (GMP). Облегчают ли новые методы, такие как генная инженерия, производство?
- Да, они снижают затраты, повышают безопасность и ускоряют производство, особенно рекомбинантных вакцин, таких как вакцины против гепатита B.
Почему так важен контроль?
Поскольку вакцины напрямую связаны со здоровьем населения, ошибка может привести к серьёзным последствиям, поэтому необходим постоянный контроль на каждом этапе.